“如果生命是一本已经写好的书,我们有没有可能,去修改里面的错别字呢?”这个充满想象力的问题,即将在一场别开生面的科普中得到生动解答。我们将带你一同探索获得诺贝尔奖的CRISPR基因编辑技术如何与实验动物携手,开启生命科学的新纪元。
1、神奇工具箱
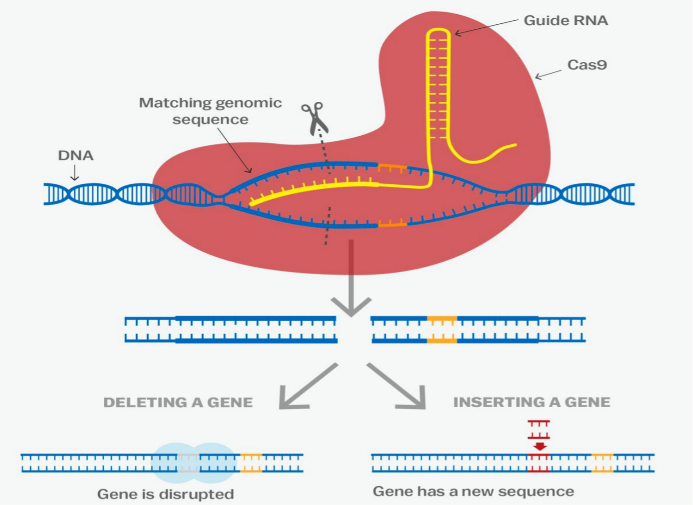
想象一下,如果有一把“分子剪刀”,能够精准找到生命之书上的错字并进行修改,那会怎样?这并非科幻,而是现实。
科学家们从细菌的防御系统中找到了一套神奇工具箱:Cas9“剪刀手”、gRNA“导航员”和DNA“目标长链”[1]。它们配合起来,就像派出一位带着精准导航的机器人,在数十亿碱基组成的生命长链上找到特定位置,完成精准编辑。
2、生命的考验

然而,在试管中剪裁DNA是一回事,在复杂的生命体内操作完全是另一回事。这就好比你能轻松修剪一段毛线,但你能在一台高速运转的精密纺织机上,只修改一根指定线头而不影响其他吗?

这把“基因剪刀”在活生生的动物体内是否安全有效?这是它从实验室走向应用必须回答的关键问题[2]。为此,三位动物朋友登场了,它们将带领这把剪刀闯过三重关键考验。
3、第一关:小鼠侠

首先登场的是 “小鼠侠”,它的超能力是 “速度”。以前,科学家想培育特定疾病的小鼠模型进行研究,过程如同大海捞针,耗时数年。现在,有了CRISPR技术,几周内就能“定制”出心脏病、糖尿病等疾病模型小鼠,极大加快了新药和疗法的研发进程[3]。例如,通过编辑特定基因,研究者能快速构建出模拟人类心血管疾病的小鼠模型,用于药物筛选[4]。
4、第二关:斑马鱼侠

接着是“斑马鱼侠”,它的绝技是“透明”。
斑马鱼的胚胎和幼鱼身体透明,当用CRISPR编辑它的基因后,科学家能够像观看高清直播一样,直接观察它的心脏如何跳动、大脑如何发育[5]。这为理解基因在活体中的功能打开了无可替代的窗口。研究者利用这一特性,实时揭示了多个基因在胚胎早期发育中的关键作用[6]。
5、第三关:猴哥

最后是“猴哥”,它代表的是“最接近人类的终极测试”。
猴子与人类在生理和遗传上高度相似。在这一关的测试,是为了确保基因编辑技术在更接近人类的复杂系统中足够安全有效[7]。这是通往人类医学应用前最为关键和谨慎的一步。例如,在灵长类动物中进行的基因编辑研究,为治疗人类肌肉萎缩症等疾病提供了关键的安全性数据[8]。
6、技术超能力
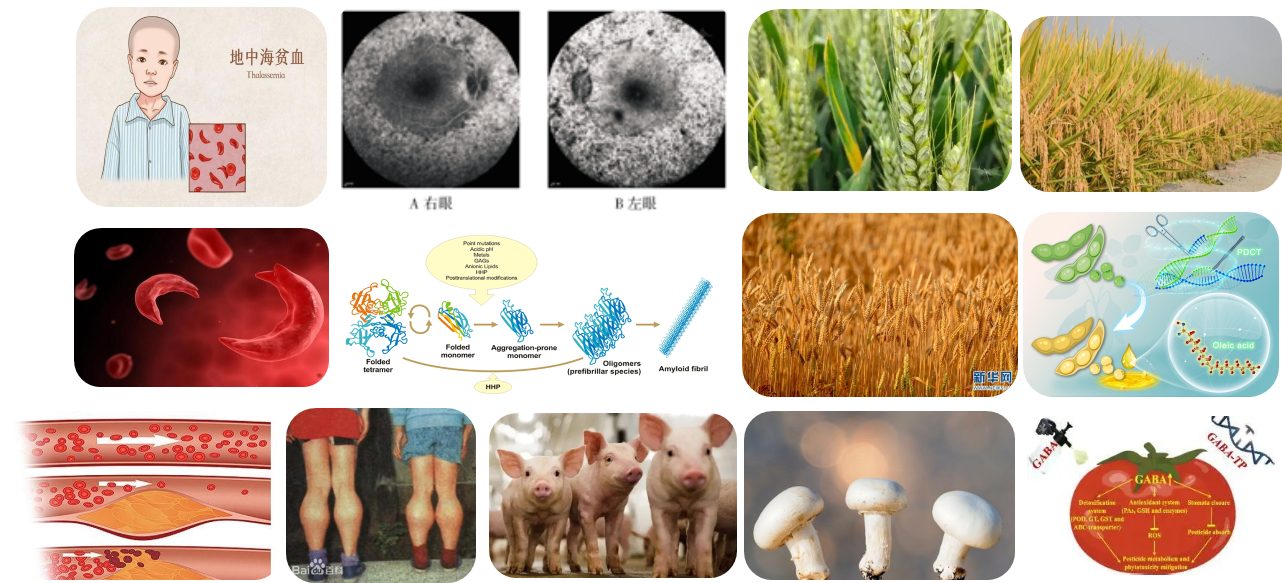
闯过重重关卡后,这把基因剪刀正在多个领域展示它的“超能力”:在医疗领域,它已帮助开发出能够“功能性治愈”镰刀型细胞贫血等重疾的疗法(相关药物Casgevy已获FDA批准)[9];在农业领域,它培育出了更健康、高产的食物,如高油酸大豆(已在美国商业化)[10];在基础科研中,它正帮助我们逐个破解基因的奥秘。
7、力量与责任

然而,越是强大的力量,就意味着越重大的责任。基因编辑技术如同一架天平:一端是治愈疾病、消除痛苦的巨大希望;另一端则是我们必须严肃思考的技术边界、社会公平和生态安全等问题。技术本身并无对错,但如何使用它,考验着全人类的智慧与规则。国际科学界已就人类生殖细胞基因编辑的审慎应用达成重要共识。
8、背后的英雄

因开发了精准基因编辑技术,Emmanuelle Charpentier 和 Jennifer A. Doudna 共同获得了2020年诺贝尔化学奖。这个故事背后,我们不仅要感谢诺贝尔奖得主的智慧发现,更要深深致敬那些沉默而伟大的 “试刀人”和“伙伴”——实验动物。正是它们的贡献,在理论突破与生命应用之间,架起了一座不可或缺的坚实桥梁。
科学的每一次飞跃,都离不开生命的托举。

参考文献:
[1] JINEK M, CHYLINSKI K, FONFARA I, HAUER M, DOUDNA J A, CHARPENTIER E. A programmable dual-RNA–guided DNA endonuclease in adaptive bacterial immunity[J]. Science, 2012, 337(6096): 816-821.
[2] DOUDNA J A, CHARPENTIER E. The new frontier of genome engineering with CRISPR-Cas9[J]. Science, 2014, 346(6213): 1258096.
[3] WANG H, YANG H, SHIVALILA C S, DAWLATY M M, CHENG A W, ZHANG F, JAENISCH R. One-step generation of mice carrying mutations in multiple genes by CRISPR/cas-mediated genome engineering[J]. Cell, 2013, 153(4): 910-918.
[4] YANG H, WANG H, SHIVALILA C S, CHENG A W, SHI L, JAENISCH R. One-step generation of mice carrying reporter and conditional alleles by CRISPR/cas mediated genome engineering[J]. Cell, 2013, 154(6): 1370-1379.
[5] HWANG W Y, FU Y, REYON D, MAEDER M L, TSAI S Q, SANDER J D, PETERSON R T, YEH J R J, JOUNG J K. Efficient genome editing in zebrafish using a CRISPR-cas system[J]. Nature Biotechnology, 2013, 31(3): 227-229.
[6] IRION U, KRAUSS J, NÜSSLEIN-VOLHARD C. Precise and efficient genome editing in zebrafish using the CRISPR/Cas9 system[J]. Development (cambridge, England), 2014, 141(24): 4827-4830.
[7] NIU Y, SHEN B, CUI Y, CHEN Y, WANG J, WANG L, KANG Y, ZHAO X, SI W, LI W, XIANG A P, ZHOU J, GUO X, BI Y, SI C, HU B, DONG G, WANG H, ZHOU Z, LI T, TAN T, PU X, WANG F, JI S, ZHOU Q, HUANG X, JI W, SHA J. Generation of gene-modified cynomolgus monkey via Cas9/RNA-mediated gene targeting in one-cell embryos[J]. Cell, 2014, 156(4): 836-843.
[8] CHEN Y, ZHENG Y, KANG Y, YANG W, NIU Y, GUO X, TU Z, SI C, WANG H, XING R, PU X, YANG S H, LI S, JI W, LI X J. Functional disruption of the dystrophin gene in rhesus monkey using CRISPR/Cas9[J]. Human Molecular Genetics, 2015, 24(13): 3764-3774.
[9] FRANGOUL H, ALTSHULER D, CAPPELLINI M D, CHEN Y S, DOMM J, EUSTACE B K, FOELL J, DE LA FUENTE J, GRUPP S, HANDGRETINGER R, HO T W, KATTAMIS A, KERNYTSKY A, LEKSTROM-HIMES J, LI A M, LOCATELLI F, MAPARA M Y, DE MONTALEMBERT M, RONDELLI D, SHARMA A, SHETH S, SONI S, STEINBERG M H, WALL D, YEN A, CORBACIOGLU S. CRISPR-Cas9 gene editing for sickle cell disease and β-thalassemia[J]. The New England Journal of Medicine, 2021, 384(3): 252-260.
[10] HAUN W, COFFMAN A, CLASEN B M, DEMOREST Z L, LOWY A, RAY E, RETTERATH A, STODDARD T, JUILLERAT A, CEDRONE F, MATHIS L, VOYTAS D F, ZHANG F. Improved soybean oil quality by targeted mutagenesis of the fatty acid desaturase 2 gene family[J/OL]. [2026][2026-01-06].