大家好!今天,我要带大家认识一位抗癌战场上的“幕后功臣”——它没有惊天动地的壮举,却用小小的身躯撑起了诺奖级的医学突破,它就是实验室里的抗癌小鼠。接下来,就让我们一起走进“小鼠与癌症免疫疗法”的奇妙故事。

一、癌症疗法
传统疗法:手术切、化疗毒、放疗烧,“杀敌一千,自损八百”。
免疫疗法:能不能让我们身体里的免疫细胞自己去打癌细胞?答案是:可以。这个看似天马行空的想法,最终催生了拿下诺奖的癌症免疫疗法,也彻底改变了人类抗癌的格局。
二、实验室里的“抗癌小鼠”
小鼠为什么是“天选之子”?
(1)基因相似度超高:小鼠和人类的基因相似度超过90%,癌细胞在小鼠体内的生长规律,和在人体里特别像。
(2)性价比高:繁殖快、饲养成本低,能快速批量“上岗”,帮科学家做大量重复实验。
(3)定制化选手:科学家能给小鼠 “装” 上人类的癌细胞,打造专属的 “癌症小鼠模型”,精准测试疗法效果。
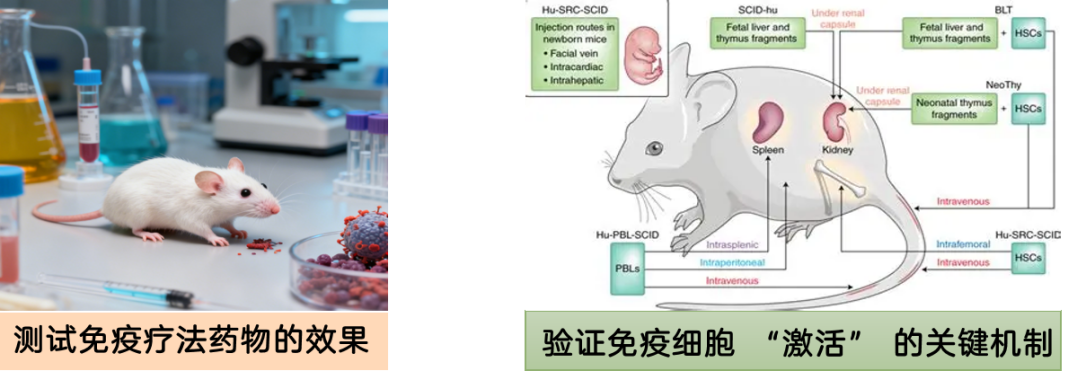
这些抗癌小鼠的 “工作内容” 也很明确,一方面测试免疫疗法药物的效果,判断哪种方案更有效;另一方面验证免疫细胞“激活”的关键机制,帮科学家找到抗癌的核心靶点。
三、诺奖级发现——“松开” 免疫细胞的“刹车”
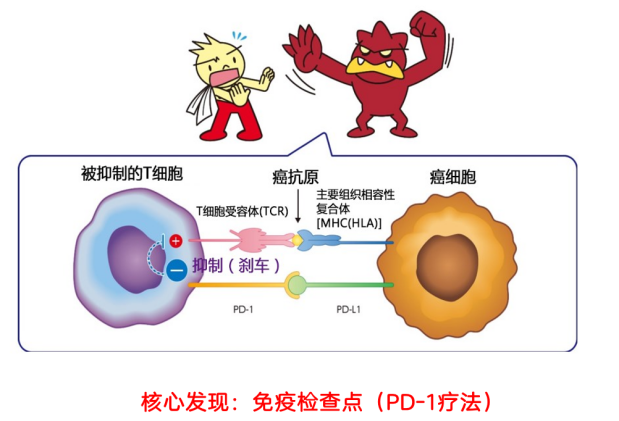
(1)2018年诺奖:发现免疫系统的“刹车”

2018年诺贝尔生理学或医学奖授予美国科学家詹姆斯·艾利森和日本科学家本庶佑,以表彰他们在癌症免疫治疗方面的贡献。他们发现我们的的免疫系统里藏着“刹车”,也就是免疫检查点。癌细胞特别狡猾,会利用这个“刹车”让免疫细胞“失明”,认不出自己,从而躲过攻击。而小鼠实验验证了这个关键猜想:科学家给患癌小鼠使用“抗刹车”药物PD-1抑制剂,奇迹发生了!小鼠体内的免疫细胞瞬间“苏醒”,疯狂攻击癌细胞,肿瘤慢慢缩小甚至消失。这个实验直接奠定了免疫检查点疗法的基础,也让2018年的诺奖实至名归。小鼠体内的免疫细胞瞬间“醒”了过来,疯狂攻击癌细胞,没多久,肿瘤竟然缩小,甚至直接消失了!这个实验,直接证明了免疫疗法是有效的,无数患者的生命因此被改写。
(2)2025年诺奖:发现免疫“刹车”Treg细胞,开辟自身免疫疾病治疗新纪元
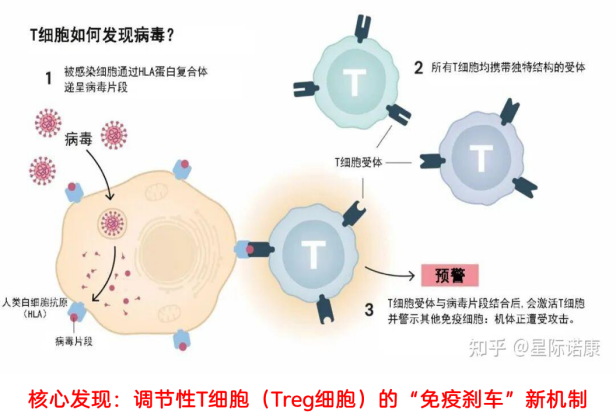
时隔7年,2025年的诺贝尔生理学或医学奖再次颁给了免疫领域。三位科学家因发现外周免疫耐受机制获奖,核心就是找到了另一种“免疫刹车”——调节性Treg细胞。

简单来说,T细胞就像免疫系统的“士兵”,能通过受体识别被病毒或癌细胞感染的细胞。而Treg 细胞的作用是“维稳”,防止免疫细胞过度激活攻击自身。但在肿瘤环境中,癌细胞会“策反”Treg细胞,让它的“刹车”功能异常亢进,反而抑制抗癌免疫反应,这一发现也为自身免疫病和癌症治疗开辟了新赛道。
四、从小鼠到人类——诺奖的诞生与 2025新进展
从实验室里的小鼠实验,到真正惠及人类患者,这中间离不开无数科研工作者的努力,也催生出了2025年的新进展:
1、给 CAR-T 细胞装 “信号放大器”
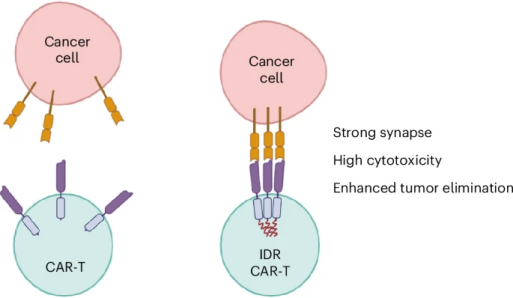
时间来到2025年,小鼠又立新功!以前 CAR-T 细胞总找不到“伪装”的癌细胞,科学家给它装了个“信号放大器”,先在小鼠身上测试,结果发现:改良后的 CAR-T,连最难搞的低抗原肿瘤都能精准消灭,血癌、实体瘤都更不在话下!

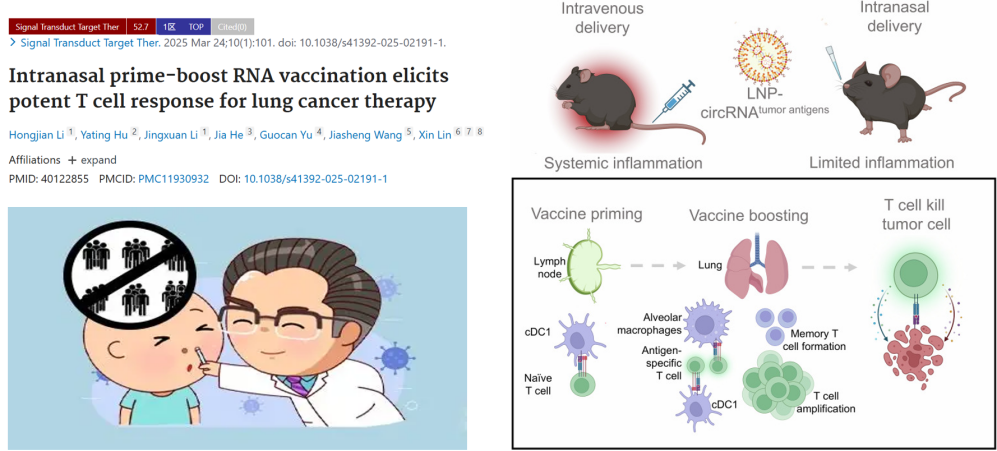
2、中国研究团队开发出全球首个鼻内给药的circRNA癌症疫苗
中国研究团队开发的全球首个鼻内给药的circRNA癌症疫苗。传统疫苗给药可能引发全身炎症,而这款鼻内疫苗通过鼻腔递送,能精准激活肺部淋巴系统的免疫反应。在小鼠实验中,它能有效诱导抗原特异性T细胞增殖,还能形成免疫记忆,既减少了全身副作用,又提高了肺癌治疗的针对性。
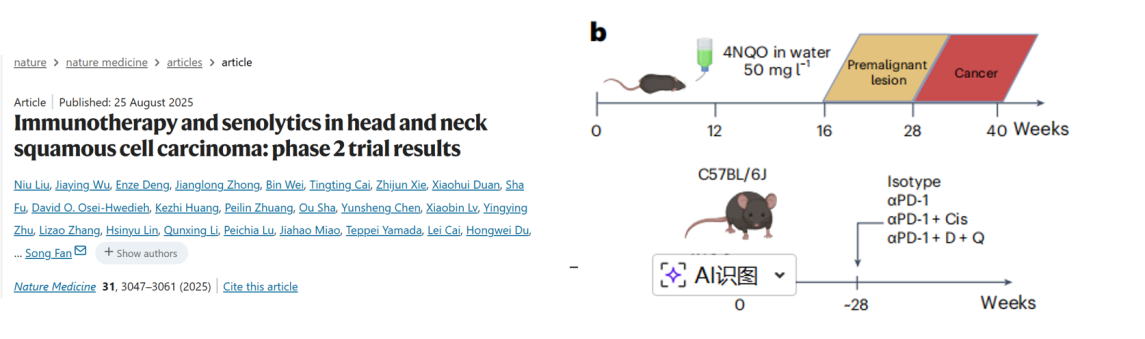
3、给免疫细胞“减龄”,破解治疗耐药难题
很多患者对免疫疗法耐药,核心原因是免疫细胞“老了”,失去了战斗力。中国科学家开展的二期临床试验发现,将PD-1抑制剂与抗衰老药物达沙替尼、槲皮素联合使用,能让“衰老”的免疫细胞重新“年轻”起来。在小鼠模型和临床患者中,都观察到肿瘤显著缩小,生存期大幅延长,为耐药患者带来了新希望。
从2018年免疫检查点疗法,到2025年Treg细胞机制发现与三大新进展,每一步突破的背后,都离不开实验小鼠的默默付出。它们是诺奖发现的“奠基者”,是新药研发的“试金石”,更是人类健康的“幕后功臣”。希望通过这个故事,大家能记住这些小小的抗癌功臣。也让我们继续尊重实验动物,铭记它们的贡献,在科研道路上不断前行,为攻克癌症、守护健康不懈努力!
参考文献:
[1] Zhang X, Xiao Q, Zeng L, Hashmi F, Sato K, Hartwich TMP, Mansolf M, Yang-Hartwich Y, Su X. IDR-induced CAR condensation improves the cytotoxicity of CAR-Ts against low-antigen cancers. Nat Chem Biol. 2025 Sep 29.
[2] Li H, Hu Y, Li J, He J, Yu G, Wang J, Lin X. Intranasal prime-boost RNA vaccination elicits potent T cell response for lung cancer therapy. Signal Transduct Target Ther. 2025 Mar 24;10(1):101.
[3] Liu N, Wu J, Deng E, Zhong J, Wei B, Cai T, Xie Z, Duan X, Fu S, Osei-Hwedieh DO, Huang K, Zhuang P, Sha O, Chen Y, Lv X, Zhu Y, Zhang L, Lin H, Li Q, Lu P, Miao J, Yamada T, Cai L, Du H, Baca SC, Huang Q, Ferrone S, Wang X, Xu F, Fan X, Fan S. Immunotherapy and senolytics in head and neck squamous cell carcinoma: phase 2 trial results. Nat Med. 2025 Sep;31(9):3047-3061.
[4] Ishida Y, Agata Y, Shibahara K, Honjo T. Induced expression of PD-1, a novel member of the immunoglobulin gene superfamily, upon programmed cell death. EMBO J. 1992 Nov;11(11):3887-95.
[5] Leach DR, Krummel MF, Allison JP. Enhancement of antitumor immunity by CTLA-4 blockade. Science. 1996 Mar 22;271(5256):1734-6.