我校药学院科研团队在在国际知名催化学期刊《ACS Catalysis》发表研究成果
稿件来源:药学院 发布时间:2025-12-23 点击次数:
近日,我校药学院宋恒教授(特聘)团队联合班树荣教授团队在国际知名催化学期刊《ACS Catalysis》(中国科学院一区TOP期刊,影响因子13.1)在线发表题为“Enzyme Engineering and Cofactor Recycling Enable Efficient Biosynthesis of Neuroactive 3α-OH-5βH Steroids with C3 Glycosylation”的研究论文(doi: 10.1021/acscatal.5c06187)。该研究构建了高效多酶级联反应体系,为神经活性3α-OH-5βH甾体及其糖基化衍生物的绿色合成提供了全新策略。我校药学院2022级硕士研究生李郑文为论文第一作者,宋恒教授和班树荣教授为共同通讯作者。
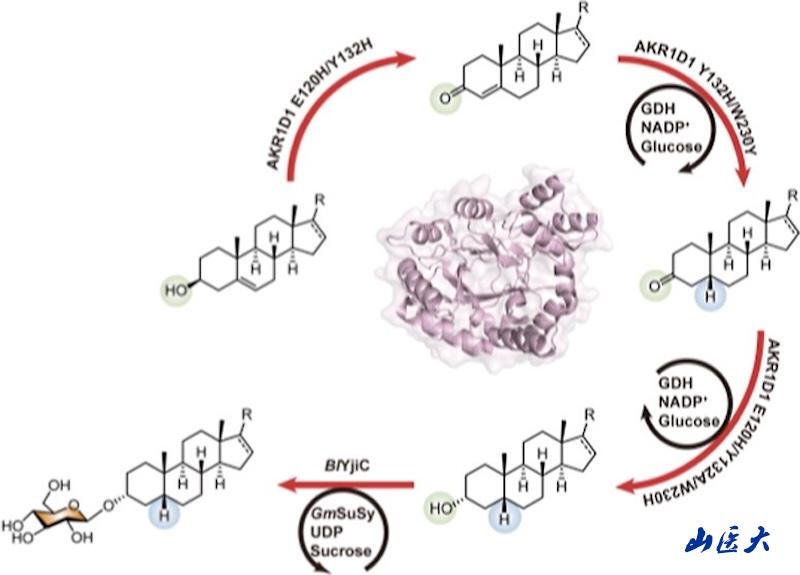
甾体类化合物是一类具有广泛生理活性的重要生物分子,在抗炎、抗癌、免疫调节等方面发挥着关键作用,其中,5β-二氢甾体及其下游代谢产物3α-OH-5βH甾体具有显著的神经活性和子宫收缩抑制作用,是多种临床药物的核心骨架。团队以人源醛酮还原酶AKR1D1为核心,通过酶工程改造策略,成功解决了天然酶催化效率低、底物兼容性有限等关键问题。研究发现,AKR1D1的E120H单点突变可完全丧失其5β-还原酶活性,同时获得羟基类固醇脱氢酶(HSD)活性。在此基础上,团队进一步对活性位点关键残基Y132和W230进行定点突变,构建的双突变体M8和三突变体M16的催化效率(kcat/Km)分别提升了7.8倍和20.7倍,关键还原反应产率分别达到94%和62%。
为实现可持续催化,团队整合葡萄糖脱氢酶(GDH)介导的辅因子再生系统,通过“单酶双构象”的创新设计,仅利用野生型AKR1D1及其E120H突变体便完成了三步连续催化反应,成功构建了从3β-OH-Δ5甾体前体到3α-OH-5βH甾体的通用生物合成途径,实现了五种目标化合物的高效合成,产率介于68%-94%之间。
考虑到甾体类化合物水溶性差的特性,团队进一步开发了YjiC糖基转移酶/SuSy蔗糖合酶耦合的C3位糖基化系统,利用廉价蔗糖作为糖供体再生UDP-葡萄糖,糖基化产物分离产率高达81%-93%,不仅显著提升了化合物的水溶性和生物利用度,还降低了生产成本,为其后续药物研发奠定了坚实基础。
该研究通过酶工程改造、辅因子再生与级联反应设计的有机结合,建立了复杂甾体化合物绿色高效的合成新方法,突破了传统化学合成的诸多局限,为甾体类药物的工业化生产提供了新的技术路线,具有重要的科学价值和应用前景。
(图文/班树荣)
复审复校:李薇
终审终校:侯小宝
发布:倪彦佩




















