医学影像学院博士研究生蔡雯雯利用近红外二区荧光/光声双模态成像探针活体示踪干细胞并实现干细胞治疗急性肝损伤的可视化研究
2020年9月23日医学影像学院博士研究生蔡雯雯在Biomaterials Science杂志上发表了题为“NIR-II FL/PA dual-modal imaging long-term tracking of human umbilical cord-derived mesenchymal stem cells labeled with melanin nanoparticles and visible HUMSC-based liver regeneration for acute liver failure”的研究论文,通过构建一种新型的近红外二区荧光(NIR-II FI)/光声(PAI)双模态成像探针MNP-PEG-H2,将其作为一种活体干细胞示踪剂,在体外标记hUMSCs后进行长期活体示踪,并实现hUMSCs治疗急性肝损伤过程的可视化和疗效评估。
荧光成像(FI)因其高灵敏度和特异性,且能实现实时无创成像而在生物医学领域中广泛应用,目前广受关注的NIR-II FI (1000-1700 nm)能够最大限度的降低生物组织产生的光子散射和自发荧光,相比于传统荧光成像和近红外一区荧光成像,组织穿透程度(〜10 mm)更深、信噪比更高、空间分辨率更好。光声成像是近年来一种新兴的无创成像手段,整合了传统光学成像卓越对比度和超声成像高时空分辨率的优势,已在临床前进行了广泛的研究并迅速向临床应用转化。在生物体内,既可依赖诸如黑色素、血红蛋白和脂质等内源性色素团产生的组织内光声信号差异进行成像,也可以使用外源性分子显像剂提高靶组织或器官的对比度和分辨率成像。NIR-II FI和PAI的结合为开发用于临床疾病成像、靶向治疗、疗效评估以及预后监测等功能的多模态探针提供了新策略。本研究用NIR-II小分子荧光染料H2对人体内源性黑色素纳米颗粒进行标记,构建了一种生物相容性好且集NIR-II FI和PAI为一体的多功能纳米探针MNP-PEG-H2。
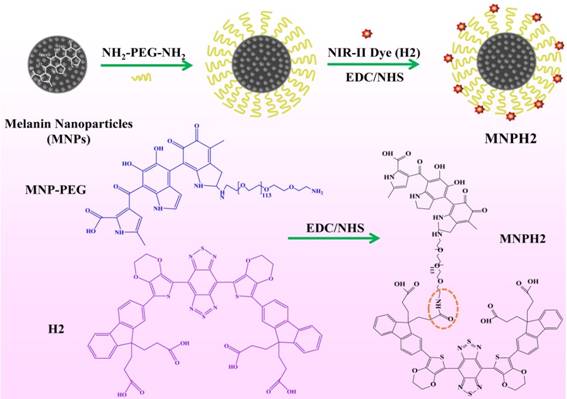
图1 MNP-PEG-H2的合成模式图及分子结构式
急性肝损伤以肝细胞广泛坏死、进展性多器官损伤和其他严重的并发症为特点,严重威胁着人类生命健康,为临床寻求一种更实用的急性肝损伤治疗方法,对于提高急性肝损伤治愈率具有重要意义。间充质干细胞是一类具有自我更新能力、多向分化潜能的细胞,在急性肝损伤治疗中具有巨大的潜力。本研究通过MNP-PEG-H2在体外标记hUMSCs后,对其在体外行NIR-II FI和PAI观察到由细胞发出的荧光和光声信号,而将细胞经由皮下注射的方式移植入裸鼠活体后,通过NIR-II FI和PAI双模态成像长期进行移植细胞的监测,直至第21天,由细胞内的MNP-PEG-H2产生的信号才接近消失。在对乙酰氨基酚成功构建小鼠急性肝损伤模型后,将标记后的hUMSCs经尾静脉注射入小鼠的血液循环系统中,在NIR-II荧光和PA图像中均能够观察到hUMSCs在肝脏组织中发生定植,且在注射6小时左右肝脏中聚集的hUMSCs的细胞数量最多,且发现一部分hUMSCs会经肝-肠轴代谢排出体外。同时通过对小鼠的体重变化情况、血清中ALT和AST水平以及肝脏组织的病理学分析,MNP-PEG-H2标记的hUMSCs在进入活体后发挥了很好的治疗效果,能够促进肝脏再生和修复急性肝损伤。
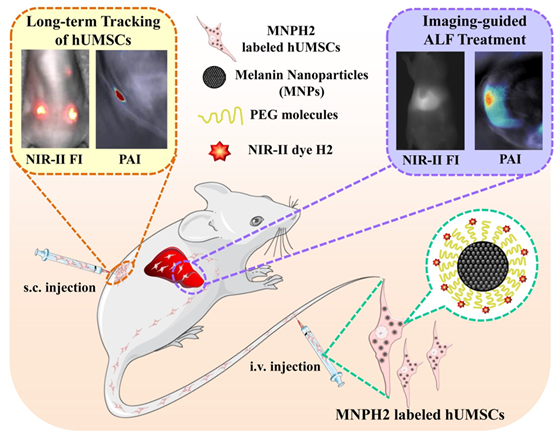
图2 MNP-PEG-H2在hUMSCs活体长期示踪和和治疗急性肝损伤的应用示意图
本研究所构建的MNP-PEG-H2纳米颗粒具有合成工艺简单,生物相容性和安全性好,良好的稳定性等优良性能,可作为一种NIR-II FI和PAI双模态示踪剂进行干细胞活体监测。