第二临床医学院王蓓课题组揭示了CB1受体拮抗剂利莫那班对阻塞性睡眠呼吸暂停介导的肾脏损伤具有保护作用
据2020年最新流行病学统计,我国阻塞性睡眠呼吸暂停(Obstructive sleep apnea, OSA)的患者已达1.76亿,且高发人群为30-60岁的中年人群。国内外研究已证实OSA是导致多器官损伤独立的、可被纠正的、重要的诱发因素之一,其对生活及健康的负面影响极大。多数OSA患者可出现严重的器官损伤,如:心、脑血管意外、糖尿病、肿瘤及肾脏疾病等。慢性间歇性低氧(Chronic intermittent hypoxia,CIH)是OSA的主要病理特征,能产生众多靶器官的严重损害,所以CIH被认为是多种疾病的独立危险因素。过去20年越来越多的证据表明,未经治疗的OSA患者患慢性肾病(Chronic kidney disease, CKD)的风险增加。最近的研究表明,OSA可通过肾内缺氧促进CKD的发生。因此,为OSA介导的CKD开发一种新的药物将对改善临床治疗效果、减少患者经济负担产生重大影响。
最近的研究表明,CIH可以通过调节线粒体功能引起靶器官损伤。由于高能量需求,肾小管上皮细胞富含线粒体,因此线粒体在肾脏疾病发病机制中所发挥的作用成为近年来的研究热点。之前的研究表明,线粒体损伤和线粒体氧化应激可以导致肾小管细胞损伤,并在肾脏疾病中诱导细胞凋亡。线粒体是活性氧(Reactive oxygen free radical species,ROS)产生的主要来源。过量的ROS会导致氧化应激和线粒体功能障碍,引起细胞衰老、损伤和凋亡。线粒体还是动态的细胞器,其不断发生分裂和融合,以维持一个健康的线粒体池。线粒体动力学受到促融合有丝分裂融合蛋白:丝裂融合蛋白1和2(Mitofusins 1 and 2, Mfn1、Mfn2)、视神经萎缩(Optical atrophy,OPA1)以及促分裂蛋白:动力相关蛋白1(Dynamin related protein 1, DRP1)、线粒体裂变蛋白1(Mitochondrial fission 1, Fis1)的精细调节。P66Shc是属于ShcA家族的一种衔接蛋白,一些研究表明,p66Shc激活和磷酸化可诱导线粒体断裂,能增加分裂蛋白和凋亡因子之间的相互作用,并激活下游凋亡途径。
因此,识别CIH中调节线粒体动力学并导致肾脏疾病和肾功能紊乱的分子对于实施治疗策略至关重要。最近的研究为大麻素受体1(Cannabinoid receptor 1,CB1R)提供了新的思路,有报道称它可能通过调节肾脏线粒体动力学影响线粒体功能。目前,CB1R拮抗剂已被用于抑制CB1R的过度表达,但这些拮抗剂是否能减轻或预防CIH介导的肾脏损伤尚不清楚。我们的前期研究证实CIH条件下可引起机体CB1R表达的增高,那么我们推测CIH可能通过增加CB1R的表达进而引起线粒体动力学异常从而导致肾脏损伤。因此,我们建立了OSA的动物模型-CIH模型,还通过体内实验检测了大鼠肾组织中CB1R、p66Shc及线粒体动力学相关蛋白Fis1、Mfn1表达的变化,以及给予CB1R拮抗剂利莫那班(Ri)靶向封闭CB1R后检测上述各指标表达的变化,观察用药前后肾组织病理及肾小管上皮细胞线粒体形态、功能情况,证实该药可以通过调节线粒体动力学减轻OSA诱导的肾脏损伤。
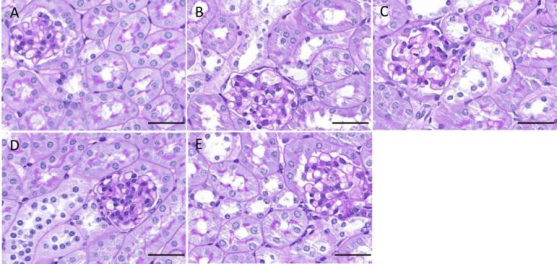
图1.各组大鼠肾脏组织PAS染色代表性图片
A:NC组;B:4w CIH组;C:6w CIH组;D:4w CIH+Ri组;E: 6w CIH+Ri组

图2.各组大鼠肾小管上皮细胞线粒体的透射电镜代表性图像
A:NC组;B:4w CIH组;C:6w CIH组;D:4w CIH+Ri组;E: 6w CIH+Ri组
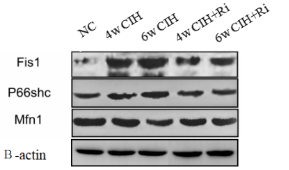
图3.各组大鼠肾脏组织Fis1、p66shc、Mfn1的 Western blot 代表性图像
该系列研究成果由王蓓教授团队完成。文章发表在《BMC nephrology》杂志上,第一作者是博士生赵莉。