口腔医学院任秀云教授课题组发现TET2在P.g-LPS促进GSDMD介导人脐静脉内皮细胞焦亡中的作用机制
近年来,随着日常生活方式的改变和老龄化进程的加速,心血管疾病的发病率不断攀升,并逐渐呈现年轻化的趋势。越来越多的研究表明,牙周炎与心血管疾病之间具有双向促进关系。牙龈卟啉单胞菌(Porphyromonasgingivalis,P.g)作为牙周炎的主要致病菌,通过进入血循环引起菌血症和内毒素血症,诱发长期、低度的慢性炎症和免疫反应,成为心血管疾病的重要危险因素。但目前牙周炎与心血管疾病发生之间的因果关系,以及牙周致病菌促进血管炎性损伤和功能障碍的直接分子机制尚未阐明。
病原菌感染诱发gasdermin D (GSDMD)依赖的细胞焦亡,一方面可以促进细胞死亡,另一方面可以触发“训练免疫”,引起“细胞因子风暴”,导致高度的炎症和免疫级联反应,成为血管炎性损伤和功能障碍的关键驱动因素,并与心血管疾病的高死亡率相关。近年来,TET甲基胞嘧啶双加氧酶2 (tet methylcytosine dioxygenase 2,TET2)在细菌脂多糖(LPS)诱导炎症和免疫内环境稳态的基因表达调控中发挥着重要的作用。本研究结果表明P. g-LPS促进血管内皮细胞焦亡与TET2的下调有关。
本研究首先在体外构建P. g-LPS诱导人脐静脉内皮细胞(Human Umbilical Vein Endothelial Cells,HUVECs)焦亡的模型。其次,评估P. g-LPS对TET2蛋白质表达的影响。最后,通过TET2敲低和过表达进一步探索TET2在P. g-LPS诱导血管内皮细胞焦亡中的作用及其对GSDMD裂解的影响。
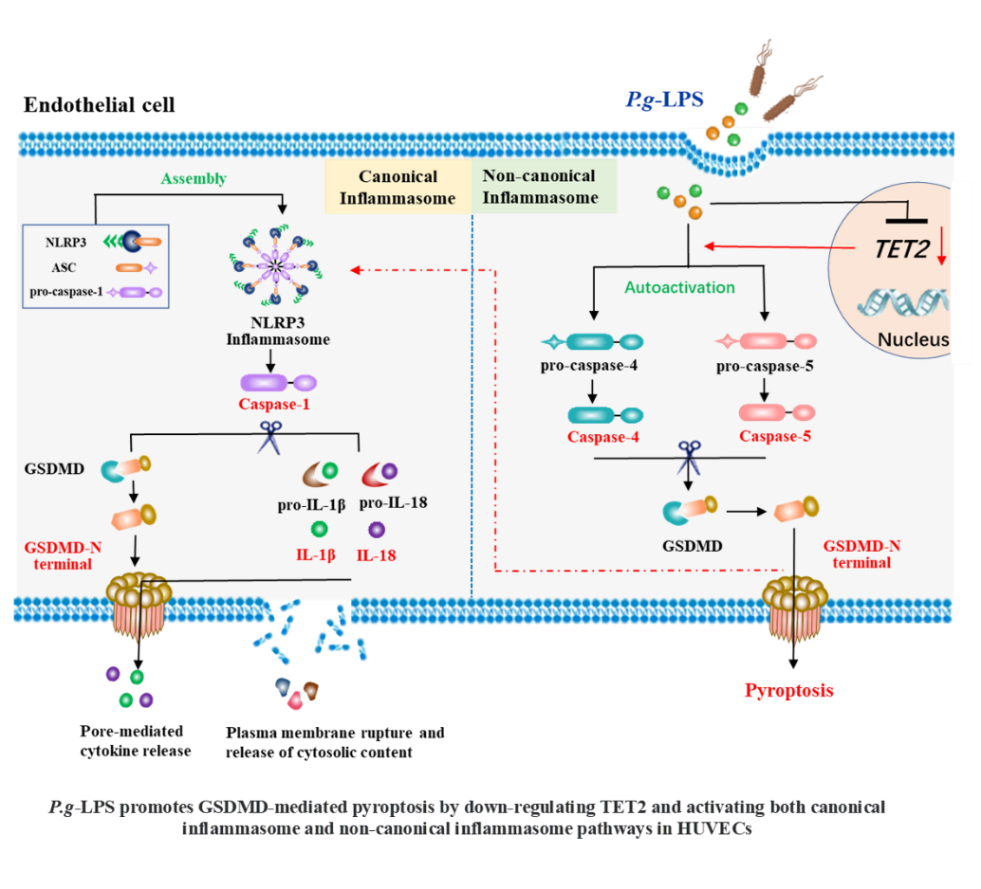
我们的研究结果聚焦于牙周致病菌对血管内皮细胞的直接影响,证明了P. g-LPS通过下调TET2激活经典炎症小体和非经典炎症小体双重途径激活GSDMD,促进HUVECs焦亡和炎性损伤。而TET2过表达可部分逆转P. g-LPS促进HUVECs焦亡的作用。明确了TET2在牙周感染促进血管内皮细胞焦亡炎性损伤中的作用,为牙周炎与心血管疾病之间的因果关系提供了新的科学基础理论依据和潜在的临床防治策略。
本课题正以山西医科大学口腔医学院任秀云教授为通讯作者,山西医科大学口腔医学院硕士研究生徐小江为第一作者撰写学术论文。该工作得到国家自然科学基金、山西省高等学校优秀成果培育项目等多方资助。